
|

|
|
����NITROGEN��Դ��mitron��gen����Ϊ����ʯ���γɡ���1772�귢�֣��ڿ�����ռ�ٷ�֮��ʮ����������塣�������ʲ������ã�Ȼ�����Ļ�����ȴ���������õġ�Ц������TNTըҩ�����ַ����Լ�������ȩ��������ǵ����ʵĹ��ɻ���������������˵�����Dz���ȱ�ٵġ� |
���ķ��ּ�ʷ
�Դ������о������˵��ķ��֣����ķ��ֲ���һ�������ġ�����1771��1772��䣬��仯ѧ�����գ�Scheele K W,1742��1786�������Լ���ʵ�飬��ʶ�������������ֱ˴˲�ͬ�ijɷ���ɵģ���֧��ȼ�յġ���������Ͳ�֧��ȼ�յġ���Ч�Ŀ�������1772��Ӣ����ѧ�ҿ��ĵ�ʲ��Cavendish H,1731��1810��Ҳ���������������������Ϊ����Ϣ�Ŀ���������ͬһ�꣬Ӣ����ѧ������˹���Priestley J,1733��1804��ͨ��ʵ��Ҳ�õ���һ�ּȲ�֧��ȼ�գ�Ҳ����ά�����������壬������Ϊ����ȼ�ر����˵Ŀ���������˼��˵����Ϊ��������ȼ�أ�����ʧȥ��֧��ȼ�յ�������
���ǣ����������գ����ǿ��ĵ�ʲ������˹�����û�м�ʱ�������Ƿ��ֵ��Ľ��ۡ���ˣ�������һ�㻯ѧ�����У�����Ϊ����ŷ�����������ո���ҽ����ֲ��ѧ�ҡ���ѧ�ҵ������¬ɪ����Rutherford D,1749��1819�����ֵġ�1772��9�£��������¬ɪ��������һƪ����Ӱ������ģ��С��̶��������������ۡ�������ԭ���ֱ�����Ӣ������ݡ����������������˵��������ʣ��������岻��ά�ֶ�����������Ȳ��ܱ�ʯ��ˮ���գ��ֲ��ܱ������գ����������ʣ�������������Ϊ�������������������������ġ��̶�������������Ķ�����̼����
��18����70���������û�����������ֺ�����Ϊһ�����廯ѧԪ�ء�D��¬ɪ��������˹������յ���һ�����ܵ�ʱȼ��˵��Ӱ�죬����û����ʶ�����������ǿ�����һ����ɳɷ֡���������ȼ�ر����˵Ŀ�������Ϣ�Ŀ�������Ч�Ŀ��������ƶ�û�б�������Ϊ�����������ơ�
�����������1787����������������������ѧ������ģ�����ġ���������������Nitrogenium����Ӣ��Nitrogen,�ǡ���ʯ������ߡ�����˼����ѧ����ΪN���ҹ���ĩ��ѧ�����������ڵ�һ�ΰѵ��������ʱ��д�ɡ�����������˼��˵�������嵭���˿����е�������
���ʵ�
���ڵؿ��е�����������0. 46%�����ֵ����Ե��ʷ���N2����ʽ�����ڿ����С����������к���һЩ��Ρ��������⣬��������������ʽ��������Ȼ���Ǻ��ٵģ�����ȴ�ձ�������л����У�����ɶ�ֲ����ĵ����ʺͺ������ҪԪ�ء�
���Ǵ���������������ܵ��ʵ���
1.��������
2.�����Ʊ�
3.������;
��������
���ʵ��ڳ�������һ����ɫ�������壬�ڱ�����µ������ܶ���1.25g��dm-3���۵�63K,�е�75K���ٽ��¶�Ϊ126K�����Ǹ�����Һ�������塣��ˮ�е��ܽ�Ⱥ�С����283Kʱ��һ���ˮԼ���ܽ�0.02�����N2��
�������ӵķ��ӹ��ʽΪ ,�Գɼ��й�����
,�Գɼ��й����� ���Ե��ӣ����γ������м���һ���Ҽ���
���Ե��ӣ����γ������м���һ���Ҽ��� �Գɼ�û�й��ף��ɼ��뷴���������Ƶ����������൱�ڹµ��Ӷԡ�����N2�����д�������N��N������N2���Ӿ��кܴ���ȶ��ԣ������ֽ�Ϊԭ����Ҫ����941.69kJ/mol��������N2��������֪��˫ԭ�ӷ��������ȶ��ġ�
�Գɼ�û�й��ף��ɼ��뷴���������Ƶ����������൱�ڹµ��Ӷԡ�����N2�����д�������N��N������N2���Ӿ��кܴ���ȶ��ԣ������ֽ�Ϊԭ����Ҫ����941.69kJ/mol��������N2��������֪��˫ԭ�ӷ��������ȶ��ġ�
�ɵ�Ԫ�ص�����̬-����˹������ͼҲ���Կ���������NH4�����⣬������Ϊ0��N2������ͼ�����ߵ���͵㣬���������������������ĵ��Ļ�����������N2������ѧ�ȶ�״̬��������Ϊ0��+5֮��ĸ��ֵ��Ļ������ֵ��λ��HNO3��N2��������ߣ�ͼ�е����ߣ����Ϸ�����ˣ���Щ������������ѧ���Dz��ȶ��ģ��������绯��Ӧ����ͼ��Ψһ��һ����N2����ֵ�͵���NH4+���ӡ�
�ɵ�Ԫ�ص�����̬-����˹������ͼ��N2���ӵĽṹ�����Կ���������N2�����ã�ֻ���ڸ��¸�ѹ���д������ڵ������£��������Ժ�������Ӧ���ɰ���

�ڷŵ������£������ſ��Ժ�������������һ��������

��ˮ������ܷ���Ĺ��ң������Ӧ�������������ᡣ

N2�������С�������䵪������и߾����ܵĽ��������������͵ĵ�������磺

N2�������ڳ����¾Ϳ�ֱ�ӷ�Ӧ��
6 Li + N2=== 2 Li3N
N2���������Mg ��Ca ��Sr ��Ba �ڳ��ȵ��¶������ã�
3 Ca + N2=== Ca3N2
N2�������Ҫ�ڰ��ȵ��¶Ȳ��ܷ�Ӧ��
2 B + N2=== 2 BN ������ӻ����
N2����������Ԫ�صĵ���һ��Ҫ�ڸ���1473K���¶��²��ܷ�Ӧ��
�����Ʊ�
���ʵ�һ������Һ̬�����ķ�����Ƶõģ�����1.5210pa��ѹ���ѵ���װ�������ƿ�������ʹ�á�һ���ƿ�е����Ĵ���Լ99.7% ��
ʵ�������Ʊ����������Ļ���ԭ�������ʵ��������������������������õ������¼��ַ�����
�ż��������᰷����Һ��

�������������Ȼ����ı�����Һ����ã�
NH4Cl + NaNO2 === NaCl + 2 H2O + N2��
�ǽ���ͨ�����ȵ�����ͭ��
2 NH3+ 3 CuO === 3 Cu + 3 H2O + N2��
�Ȱ�����ˮ��Ӧ��
8 NH3 + 3 Br2 (aq) === 6 NH4Br + N2��
���ظ���識��ȷֽ⣺
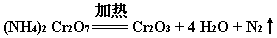
������;
����Ҫ���ںϳɰ����ɴ����컯�ʡ������ըҩ�ȣ������Ǻϳ���ά�����ڡ����ڣ����ϳ���֬���ϳ��ȵ���Ҫԭ�ϡ����ڵ��Ļ�ѧ���ԣ��������������塣�Է�ֹijЩ���屩¶�ڿ���ʱ�������������õ���������֣���ʹ��ʳ��ù�á�����ѿ�����ڱ��档Һ��������������䶳����
���ijɼ������ͼۼ��ṹ
���ڵ���N2�ڳ������쳣�ȶ������dz�����Ϊ����һ�ֻ�ѧ���ʲ����õ�Ԫ�ء�ʵ�����෴��Ԫ�ص��кܸߵĻ�ѧ���ԡ�N�ĵ縺�ԣ�3.04��������F��O��˵�����ܺ�����Ԫ���γɽ�ǿ�ļ������ⵥ��N2���ӵ��ȶ���ǡ��˵��Nԭ�ӵĻ����ԡ�������Ŀǰ���ǻ�û���ҵ��ڳ��³�ѹ����ʹN2���ӻ������������������Ȼ���У�ֲ������ϵ�һЩϸ��ȴ�ܹ��ڳ��³�ѹ�ĵ����������£��ѿ����е�N2ת��Ϊ���������Ϊ���Ϲ���������ʹ�á����Թ̵����о�һֱ��һ����Ҫ�Ŀ�ѧ�о����⡣��������б�Ҫ��ϸ�˽�ijɼ����Ժͼۼ��ṹ��
Nԭ�ӵļ۵��Ӳ�ṹΪ2s2p3������3���ɵ����Ӻ�һ�Թµ��Ӷԣ��Դ�Ϊ���������γɻ�����ʱ���������������ּ��ͣ�
1.�γ����Ӽ�
2.�γɹ��ۼ�
3.����
�γ����Ӽ�
Nԭ���нϸߵĵ縺�ԣ�3.04������ͬ�縺�Խϵ͵Ľ�������Li���縺��0.98����Ca���縺��1.00����Mg���縺��1.31�����γɶ�Ԫ������ʱ���ܹ����3�����Ӷ��γ�N3-���ӡ�
N2+ 6 Li == 2 Li3N
N2+ 3 Ca == Ca3N2
N2+ 3 Mg == Mg3N2
N3-���ӵĸ���ɽϸߣ��뾶�ϴ�171pm��������ˮ���ӻ�ǿ��ˮ�⣬��˵������ͻ�����ֻ�ܴ����ڸ�̬��������N3-��ˮ�����ӡ�

�γɹ��ۼ�
Nԭ��ͬ�縺�Խϸߵķǽ����γɻ�����ʱ���γ����¼��ֹ��ۼ���
��Nԭ�Ӳ�ȡsp3�ӻ�̬���γ��������ۼ�������һ�Թµ��Ӷԣ����ӹ���Ϊ�����ͣ�����NH3��NF3��NCl3�ȡ�
���γ��ĸ����۵���������ӹ���Ϊ���������ͣ�����NH4+���ӡ�
��Nԭ�Ӳ�ȡsp2�ӻ�̬���γ�2�����ۼ���һ��������������һ�Թµ��Ӷԣ����ӹ���Ϊ���Σ�����Cl��N=O ����Nԭ����Cl ԭ���γ�һ��������һ���м���Nԭ���ϵ�һ�Թµ��Ӷ�ʹ���ӳ�Ϊ���Ρ���
��û�йµ��Ӷ�ʱ������ӹ���Ϊ�����Σ�����HNO3���ӻ�NO3-���ӡ����������Nԭ�ӷֱ�������Oԭ���γ������Ҽ������Ħй���ϵ�һ�Ե��Ӻ�����Oԭ�ӵijɵ��е����γ�һ���������ĵ��ӵIJ�����м���������������У�����Oԭ�Ӻ�����Nԭ��֮���γ�һ�������������ӵIJ������м���
���ֽṹʹ������Nԭ�ӵı���������Ϊ+5�����ڴ��ڴ�м����������ڳ��������㹻�ȶ��ġ�
��Nԭ�Ӳ�ȡsp �ӻ����γ�һ��������������������һ�Թµ��Ӷԣ����ӹ���Ϊֱ���Σ�����N2���Ӻ�CN-��Nԭ�ӵĽṹ��
����
Nԭ�����γɵ��ʻ���ʱ���������йµ��Ӷԣ���������ĵ��ʻ�������Ϊ���ӶԸ����壬�����������λ������[Cu(NH3)4]2+��
�����⻯��
�����⻯��һ���У�
1.�� NH3
2.���� N2H4
3.�ǰ� NH2OH
4.������� HN3
��������Ҫ���ǰ������ǵ�������Ҫ������֮һ��
�� NH3
����һ���д̼���ζ����ɫ���壬���Ǵ����¼���������ܰ���
��NH3���Ʊ�
��NH3���ӵĽṹ
��NH3����������
��NH3�Ļ�ѧ����
����μ���εļ�����Ӧ
��NH3���Ʊ�
��ҵ���Ʊ������õ����������ڸ��¸�ѹ�ʹ���������ֱ�ӷ�Ӧ�ϳɵģ�

ʵ������ͨ������κ�ǿ��ķ�Ӧ���Ʊ�����������
(NH4)2SO4 (s) + CaO (s) === CaSO4 (s) + 2 NH3��+ H2O
��Щ��Σ���NH4NO3��(NH4)2 Cr2O7�ȣ����ȷֽ���ܲ������������������һ���÷������������Σ���NH4Cl��ʵ��������һ���Ʊ����ķ������õ�����ͬˮ���ã�
Mg3N2 + 6 H2O === 3 Mg(OH)2 + 2 NH3��
��NH3���ӵĽṹ
��NH3�����У�Nԭ�Ӳ�ȡ������sp3�ӻ�����һ�Թµ��ӶԺ�������Hԭ�ӽ�ϳɵĹ��۵��������ڹµ��ӶԶԳɼ����ӶԵ��ų����ã�ʹN�H��֮��ļ��ǡ�HNH �������������109��28��������107�������״������״�ġ����ֽṹʹ��NH3�������൱��ļ��ԣ�ż����Ϊ5.5��10-30C��m�������γ������
��NH3����������
NH3��������ˮ����ˮ�е��ܽ�ȱ������������嶼��273Kʱ1dm3ˮ���ܽ�1200dm3�İ���ͨ�������а���ˮ��Һ������ˮ��һ������Ũ��ˮ���ܶ���0.91gcm-3����NH3Լ28%NH3�ڳ����º����ױ���ѹҺ����Һ����һ���ܺõ��ܼ������ڷ��ӵļ��Ժʹ��������Һ���������������ʷ���ͬˮ�dz����ƣ�������Һ����ˮ���������ʣ���

NH3��H2O��ȣ����ǵIJ�����ڣ�
�� NH3�DZ�H2O��ǿ���������Լ�������˵���õĵ��ӶԸ����塣
�� NH3�ų�����H+����������H2O���ӡ�
һЩ���õĽ������Դ�ˮ���û�����������������Һ���оͲ���ô�����û��⡣��Һ���ܹ��ܽ��������һ����ɫ��Һ�����ֽ���Һ����Һ�ܹ����磬�������ֽ�ų���������ǿ��ԭ�ԡ������Ƶ�Һ����Һ��

����Һ����Һ����ɫ���ܵ��粢��ǿ��ԭ�Ե�ԭ������Ϊ����Һ�����ɡ����ϵ��ӡ���Ե�ʡ�����������ܽ���Һ����ʱʧȥ���ļ۵������������ӣ�

Ȼ��Һ������ͬ���Ӻ͵��ӷ����ܼ��Ӻ����ã�

��NH3�Ļ�ѧ����
NH3����Ҫ��ѧ���������¼������棺
����������
NH3�����еŵ��Ӷ������ںͱ�ķ��ӻ������γ���λ�������ɸ�����ʽ�İ������[Ag(NH3)2]+��[Cu(NH3)4]2+��BF3��NH3�ȶ�����NH3Ϊ��λ������
��������
NH3��������ˮ����ˮ����Ҫ�γ�ˮ�Ϸ���NH3H2O��2NH3H2O������Щˮ�����мȲ�����NH4+��OH-��Ҳ������NH4OH���ӣ������ǰ�����ͨ�����������Ϊ276pm��ͬˮ���������ӵġ���298Kʱ��0.1moldm-3 NH3ˮ��Һ��ֻ��1.34%�����������ã�

������Ӧ��ƽ�ⳣ����ʾʽ�ǣ�

����NH3ˮ��Һ�������ԡ�
NH3���Ȼ���HCl����̬��ˮ��Һ�ж���ֱ�ӻ��������Ȼ��NH4Cl ��
NH3 + HCl ==== NH4Cl
NH3������������Ҳͬ���õ���Ӧ����Ρ�
�ۻ�ԭ��
NH3���Ӻ�NH4+������N��������Ϊ-3�������һ��������������ʧȥ���Ӷ��Ի�ԭ�ԡ����磺
i.���ڿ����в���ȼ�գ�ȴ���ڴ�����ȼ�գ�
4 NH3+ 3 O2 === 6 H2O + 2 N2
�ڴ������������������£�NH3�ɱ�������NO��
4NH3+5 O2 === 4 NO + 6 H2O
�����Ӧ�ǹ�ҵ�ϳ�����Ļ�����
ii.Cl2��Br2�ڳ����£�Ҳ������̬����Һ�а�NH3�����ɵ��ʣ�
2 N H3+ 3 Cl2 === 6 HCl + N2
��Cl2������������ NCl3
NH3+ 3 Cl2 === NCl3 + 3 HCl
iii.NH3ͨ���ȵ�CuO���Ա������ɵ���N2��
2 NH3+ 3 CuO === 3 Cu + 3 H2O + N2
����������������������ã�Ҳ���ɱ������ɵ��ʵ���

iv.NH4+���ӵĻ�ԭ�Ա�NH3���Ӹ�Ϊ���ԣ������������Ժ��������Σ����Ȼᷢ�����ҷ�Ӧ������N3-��������N2����������������磺

�ȵ�HNO3��HCl �Ļ������Խ���Һ�е��������ȫ�����ɵ��������Ϊ��������Һ�е�NH4+����ʱ�������Ӧ�Ƿdz����õġ�
����μ���εļ�����Ӧ
�����һ������ɫ�ľ��壬������ˮ��NH4+��Na+�ǵȵ����壬���NH4+����+1�۽������ӵ����ʡ�NH4+�����нϴ�İ뾶148pm ��������K+133pm��Rb+148pm���ӵİ뾶��������γ�����Ρ����ͬ�����������Ƶ��ܽ�ȡ�
�����ڰ��������ԣ���ζ���һ���̶ȵ�ˮ�⣬��ǿ����ɵ���Σ���ˮ��Һ�����ԣ�
NH4Cl + H2O ==== NH3��H2O + HCl
�����κ���ε���Һ�м���ǿ����ȣ��ͻ��ͷų�NH3�����Ǽ����Ƿ�����εķ�Ӧ��

��ε���һ�ּ�������������NH4+����Һ�м�����˹���Լ������ܲ��������ĺ��ɫ������

����˹���Լ���[HgI4]2-��KOH�Ļ����Һ��
����ε�һ����Ҫ�������������ȶ��Բ��̬��μ����ֽ�Ϊ������Ӧ���

������Dz��ӷ��Եģ���ֻ�а��ӷ��ݳ����������ʽ��������������У�

�����Ӧ�����������ԣ���ֽ������NH3������������������NH4NO3���ȷֽ�ʱ��NH3��������N2O��

��������¶ȸ���573Kʱ��N2O�ַֽ�ΪN2��O2��

������Щ������ֽ�ʱ�����������ȣ��ֽ���������壬����������ܱյ������н��оͻᷢ����ը������������ʣ�NH4NO3����������ըҩ��
���� N2H4
����NH2-NH2�ֽС��¡������Կ�����NH3�����ڵ�һ��Hԭ�ӱ����� -NH2ȡ������������ӽṹ����ͼ��ʾ��

�����Ľṹ�����ڹ�������H2O2�������������Ӿ��кܴ��ԣ� ����һ��ʵ��˵������˳ʽ�ṹ����N2H4��ÿ��Nԭ���϶���һ�Ԧҹµ��Ӷԣ�N��������Ϊ-2��
����һ��ʵ��˵������˳ʽ�ṹ����N2H4��ÿ��Nԭ���϶���һ�Ԧҹµ��Ӷԣ�N��������Ϊ-2��
�������Ʊ��������ô�������NaClO��Һ����������NH3���ܵķ�Ӧ��
NaClO + 2 NH3 === N2H4 + NaCl + H2O
N2H4��һ����ɫ�ĸ߶���ʪ�ԵĿ�ȼҺ�壬��N2H4��Nԭ�ӵŵ��ӶԿ���ͬH+��϶��Լ��ԣ�������Բ���NH3ǿ��N2H4��һ����Ԫ���
N2H4��NH3һ��Ҳ��������λ�����
�ڼ�����Һ�У�N2H4�Ǹ�ǿ��ԭ�������ܽ�AgNO3��ԭ�ɵ���������Ҳ���Ա�±��������
N2H4+ 2 X2=== 4 HX + N2
N2H4�ڿ�����ȼ�ջ����������H2O2��Ӧʱ�����ܷų��������ȣ���˿��������ȼ�ϣ���������ƽ�����

�ǰ� NH2OH
�ǰ� NH2OH���Կ�����NH3�����ڵ�һ��Hԭ�ӱ��ǻ�-OHȡ������������ķ��ӽṹ����ͼ��ʾ��

������Nԭ�ӵ�������Ϊ-1��Nԭ������һ�Թµ��Ӷԡ�������һ�����ǰ���һ�ֱ����������ļ���ڹµ��ӶԵĴ��ڣ��ǰ�Ҳ������Ϊ��λ�壬������λ�����
���ǰ���һ�ֲ��ȶ��İ�ɫ���塣�ڼ�����Һ���ǰ��Ǹ���ǿ�Ļ�ԭ�����������ܰ����λ�ԭ�ɵ�������
2 NH2OH + 2 AgBr === 2 Ag + N2 + 2 HBr+ 2 H2O
2NH2OH + 4 AgBr === 4 Ag + N2O +4 HBr +H2O
�������ǰ�����ԭ�����ŵ㣬һ������������ǿ��ԭ�ԣ���һ���������ǵ���������������뷴Ӧϵͳ���������Ӧ��Һ��������ʡ�
������� HN3
����������������ʱ��������������HN3��
N2H4 + HNO2 ==== 2 H2O + HN3
���ķ��ӽṹ����ͼ��ʾ��

��HN3�����У�����Nԭ����ֱ��������H-N����N-N-N����ļн�Ϊ110.9�㣬��Ȼ����Hԭ�ӵĵ�1��Nԭ����sp2�ӻ��ģ���2�͵�3��Nԭ�Ӷ���sp�ӻ��ģ�������Nԭ�Ӽ����������� �������HN3��Nԭ�ӵ�ƽ��������Ϊ-1/3 ��N3-������һ����±���ӣ���Ӧ����������±���ӣ�����AgN3Ҳ��������ˮ�ġ�
�������HN3��Nԭ�ӵ�ƽ��������Ϊ-1/3 ��N3-������һ����±���ӣ���Ӧ����������±���ӣ�����AgN3Ҳ��������ˮ�ġ�
��HN3����ɫҺ�壬��һ�ֱ�ը����Ȼ���ײ���ͱ�ը����������������HN3��ˮ��Һ�����ȶ��ģ���ˮ�����е��룬�������������ڴ��ᣬ�Ǹ����ᡣ
����������
Nԭ�Ӻ�Oԭ�ӿ����ж�����ʽ��ϣ�����Щ�����ʽ�У�N�����������Դ�+1�䵽+5�������ֳ����ĵ����������У���һ������NO�Ͷ�������NO2��Ϊ��Ҫ��
1.һ������NO
2.��������NO2
3.һ��������N2O
4.����������N2O3
5.����������N2O5
һ������NO
��NO�����У�Nԭ�Ӳ�ȡsp �ӻ����γ�һ���Ҽ���һ���м���һ�������Ӧм���N��������Ϊ+2��NO����11���۵��ӣ�ȫ���ɶ��Dz����ܵģ����NO��һ������ӷ��ӣ���˳���Եġ�
NO��һ����ɫ���壬����ˮ������ˮ��Ӧ������ȼ������������������Ӧ���ɺ���ɫ��NO2��
2 NO + O2 ==== 2 NO2
���ڷ������йµ��Ӷԣ�����±�ؼӺϷ�Ӧ����±����������
2 NO + Cl2=== 2 NOCl
NOҲ������Ϊ��������ɽ�������������λ���������Fe2+���ɵ�����������Ǽ���������ġ���ɫ��ʵ�顱��ɫ��ԭ��
NO + FeSO4 ==== [Fe(NO)]SO4
NO��һ�����������������һ��������
ʵ�������Ʊ�NO�ķ�������ͭ��ϡ���ᷴӦ��
3 Cu + 8 HNO3(ϡ) === 3 Cu(NO3)2+ 2 NO��+ 4 H2O
��������NO2
��NO2�����У�Nԭ�Ӳ�ȡsp2�ӻ����γ������Ҽ���һ�������Ӧм���N��������Ϊ+4�����ӹ���Ϊ���Ρ�NO2����17���۵��ӣ���һ������ӷ��ӣ���˳���Եġ�
NO2��һ�ֺ���ɫ�ж������壬����ʱ�ۺϳ���ɫ��N2O4��
2 NO2 ==== N2O4
NO2������ˮ��������������������������κ��������εĻ�����һ�ֻ��������
2 NO2 + H2O == HNO3 + HNO2
2 NO2 + 2 NaOH === NaNO3 + NaNO2 + H2O
��NO��������ͭ��ŨHNO3��Ӧ�����Ʊ���NO2��
2 NO + O2 ==== 2 NO2
Cu + 4 HNO3(Ũ) === Cu(NO3)2 + 2 NO2��+ 2 H2O
һ��������N2O
N2O��һ����ɫ���壬����ζ����������ˮ��������ˮ���á�����ȼ����һ���������������������������
N2O�ķ�����ֱ���εģ�Nԭ�Ӳ�ȡsp�ӻ������������Ҽ��������������ĵ��Ӧм���N��������Ϊ+1��
����識��ȷֽ���Ʊ���N2O��

����������N2O3
N2O3�Dz��ȶ�����ɫ���壬��NO��NO2������һ��Ϳ��Եõ�N2O3��
NO (��ɫ) + NO2 (����ɫ) ==== N2O3 (��ɫ)
��ѹ��N2O3���ɷֽ�ΪNO��NO2��N2O3��һ����������������������������
N2O3���ӵĽṹ��ͼ��ʾ��

�ڷ�����Nԭ�Ӷ���ȡsp2�ӻ�������Nԭ��ͨ���ҹ��ۼ������������������д�����һ�������������ӵ�����Ĵ�м� ��N��������Ϊ+3��
��N��������Ϊ+3��
����������N2O5
N2O5��һ�ְ�ɫ���壬�׳��⣬�����ȶ����ܱ�ը�Էֽ⣬�ֽ�ΪNO2��O2���Ǹ�ǿ������������ˮ�������ᣬ���������������

N2O5����P2O5ʹHNO3��ˮ����NO2�����O3��Ӧ���Ʊ���
N2O5�����������нṹ��Nԭ����sp2�ӻ��ɼ���6���Ҽ���2���������ĵ��Ӧм� ��
��
�����ἰ����
���������ἰ���Σ��������ۣ�
1.��������Ʊ�
2.������Ľṹ
3.�����ἰ���ε�����
4.����������ӵļ���
��������Ʊ�
�ѵ�Ħ��NO��NO2�Ļ�����ܽ��ڱ�����ˮ�л������������ε�����Һ�м���ǿ��ʱ������������Һ�����������

HNO2�ܲ��ȶ��������������ϡ��Һ�У���������ʱ���ֽ��NO��NO2��H2O��
������Ľṹ
��HNO2�����У�Nԭ�Ӳ�ȡsp2�ӻ������������Ҽ���һ���м�������һ�Թµ��Ӷԣ�NO2-����Ϊƽ�������νṹ��N��������Ϊ+3��
HNO2�����ֽṹ��˳ʽ�ͷ�ʽ��һ����������ʽ�ṹ��˳ʽ�ȶ���
�����ἰ���ε�����
��HNO2�Ǹ����ᣬ�����Աȴ�����ǿ��

��������
�����ἰ������Nԭ�Ӿ����м�����̬+3����Ȼ���ǼȾ��������ԣ��־��л�ԭ�ԣ�����������Ϊ����������������������ϡ��Һʱ��NO3-���ӻ�ǿ����һ���������������Һ�еı��缫����ֵ���Կ�����
�ǻ�ԭ��
��Ȼ��������Һ��HNO2�Ǹ���ǿ�������������������������Ը�ǿ��KMnO4��Cl2��ǿ������ʱ����Ҳ���Ա��ֳ���ԭ�ԣ�������Ϊ�����Σ�

�ڼ�����Һ��NO2-�Ļ�ԭ������Ҫ�ģ������е������ܰ�NO2-������NO3-��
��NO2-�����������������

���������ξ��кܸߵ����ȶ��ԣ����ý����ڸ����»�ԭ�����εķ������Ʊ��������Σ�
Pb(��)+NaNO3====PbO + NaNO2
�������γ���ɫ��AgNO2������ˮ�⣬һ�㶼������ˮ�����������ж������°����ʡ�
����������ӵļ���
��������Һ�У�NO2-������������-�������ã�����������dz�ۺ�ɫ����Һ��֤��NO2-���ӵĴ��ڣ�

�����Ӧ���������Ũ�ȵ�NO2-���ӣ���NO2-Ũ������ʱ���ۺ�ɫ��ʧ�����ɻ�ɫ��Һ���ɫ������
���ἰ����
��������Ҫ�Ĺ�ҵ����֮һ����������ըҩ��Ⱦ�ϡ������κ�����������ѧҩƷ����Ҫԭ�ϣ��������ۣ�
1.������Ʊ�����
2.������ӵĽṹ
3.�����ǿ������
4.�����ε��Ȳ��ȶ���
5.��������ӵļ���
������Ʊ�����
����������
������������Ŀǰ��Ҫ�Ĺ�ҵ��������ķ�������1273K�Ͳ�����90%Pt��10%Rh�Ͻ�����Ϊ����ʱ��NH3���Ա������е�O2������NO��NO��һ����O2��������NO2��NO2��ˮ���վͳ�Ϊ���

����������Ƶõ�������Һ��HNO3Լ50% ����Ҫ�õ�����Ũ�ȵ��ᣬ����ϡHNO3�м�ŨH2SO4��Ϊ��ˮ����Ȼ������
����ȶ������Ȼ��ܹ���������������ֽ����ã�
4HNO3 === 2H2O + NO2 + O2
�Ƶ绡��
�ÿ���ͨ���¶�Ϊ4273K�ĵ绡��Ȼ�������Ѹ����ȴ��1473 K���£����Եõ�NO���壺

��һ����ȴ����ʹ��NO��O2���ñ��NO2��Ȼ����ˮ�����Ƴ����ᡣ�˷����ܵ�����Դ�����ơ�
����Ȼ�����ѿ�����һ����N2��O2�����һ�����ɵ��������ﱻ��ˮ���ճ���������������У��ٺ�ɳʯ�������ϳ������λ����������������ֲ�����ն�����л�������������ʵȡ����ֹ�����ֲ��ͨ���������ѿ����еĵ��̶�Ϊ��������Ĺ���һ��ά���ŵ�������Ȼ���ѭ����
����������Ũ�������÷�
��ʵ�����У�����������Ũ���ᷴӦ���Ʊ��������ᣬ�˷���ȥ�����ڹ�ҵ�����ϡ�

����HNO3��һ���ӷ����ᣬ���Դӷ�Ӧ�����������������������Ӧ��ֻ������H2SO4�е�һ���⣬��Ϊ�ڶ�����Ӧ��

��Ҫ��773K���ҷ�Ӧ����ʱHNO3��ֽ⣬����ʹ���ʽ��͡�
������ӵĽṹ
��HNO3�����У�Nԭ�Ӳ�ȡsp2�ӻ����γ������Ҽ�������Oԭ��Χ��Nԭ����ͬһƽ���ϳ�������״��
Nԭ�Ӧй���ϵ�һ�Ե��Ӻ�����Oԭ�ӵijɵ��е����γ�һ����ֱ��sp2ƽ����������ĵ��ӵIJ�����м���Nԭ�ӵı���������Ϊ+5��
��NO3-�У�ÿ����ONO������120��,Nԭ������sp2�ӻ������γ������Ҽ��⣬��������Oԭ���γ�һ���м���
�����ǿ������
ǿ�������������һ����Ҫ��ѧ���ʣ����Ǵ�
�ŷ�Ӧ����
���������Ӧ
����ǽ�����Ӧ
�����������������ǿ�����ԡ�
��Ӧ����
�����ǿ�����������ڣ�
��HNO3�е�N�����������̬+5��
�� HNO3���Ӳ��ȶ����ܹ�����ʱ��ֽ�ų�O2��NO2��

�ֽ����NO2�Է�Ӧ�д����ã�HNO3��û�ԭ���ĵ��ӣ���Ӧ�㱻���٣�

Cu��HNO3��Ӧ��������ʺ���������ӿ죬������Һ�м���NaNO2���壬�ɼӿ�Cu��HNO3�ķ�Ӧ�����⣬����HNO3�к�ǿ�������ԣ�������Ϊ�������ܽ��кܶ��NO2��Ե�ʡ���Щ��ʵ����NO2�д����õ�֤�ݡ�
������Ӧ
�������������𡢲���ҿ����ɡ��ѡ���ȣ��⣬HNO3���������������н������������Ρ����磺

�������������������ŨHNO3�Ӵ�ʱ�ᱻ�ۻ�����������һ��������������װʢŨHNO3����
ϡHNO3Ҳ�н�ǿ��������������ŨHNO3��֮ͬ������ϡHNO3�ķ�Ӧ�ٶ������������������������������ʲ��ܴﵽ�������̬������Hg22+

ŨHNO3��Ϊ������ʱ���仹ԭ�������ΪNO2�������������Ӧ���仹ԭ������N�����������Ͷ��٣���Ҫȡ�������Ũ�ȡ������Ļ����Ժͷ�Ӧ���¶ȣ���Ӧ���ӣ�����ͬʱ���ɶ��ֻ�ԭ���
��ǽ�����Ӧ
�ǽ����г�Cl2��O2��ϡ�������⣬���ܱ�ŨHNO3����������������ᣬ���磺

�л����̼�ܱ�ŨHNO3������CO2����Щ�л�������ŨHNO3��������ȼ�ա�ŨHNO3��ǽ�������ʱ�Ļ�ԭ����������NO��
�����ε��Ȳ��ȶ���
�����ε����ȶ��Բ����������Σ������������ֽ⣬�����ε��ȷֽ�������ӣ���Ҫ��Ϊ���¼��֣�
��������ͼ�����������ˮ�������ȷֽ������������κͷų�O2����

����λ˳����Mg��Cu֮��Ľ���Ԫ�ص���ˮ�������ȷֽ�ʱ������Ӧ������������磺

(��λ˳��K Na Mg Zn Fe Ni Sn Pb H Cu Hg Ag Au)
�������ε����������������������ԭ����ʱ�����ǵ���ˮ���������ȷֽ�ʱ�����ܷ�����������֮���������ԭ��Ӧ�����磺

�����нᾧˮ�����������ȷֽ�ʱ�ᷢ��ˮ�ⷴӦ�����ɼ�ʽ�Ρ���ΪHNO3�Ǹ��ӷ����ᡣ

��������ӵļ���
���Թ��м������������ε�ϡ��Һ���ټ�������Fe2+��������Һ��Ȼ�����Թܱڼ���Ũ���ᣬ����Ũ�������Һ�Ľ����Ͽ����γ�һ��ɫ��������ɫ����֤��NO3-���ڡ�

 �ղش���
�ղش��� �ղش���
�ղش���